น้ำเป็นส่วนสำคัญในชีวิตของเรา ตั้งแต่การดื่มและการปรุงอาหาร ไปจนถึงการทำความสะอาดและการใช้งานในอุตสาหกรรม อย่างไรก็ตาม น้ำแต่ละชนิดก็ไม่ได้เหมือนกัน ในหลายพื้นที่ น้ำที่ไหลออกมาจากก๊อกน้ำจะถูกจัดเป็นน้ำกระด้าง ซึ่งเป็นน้ำที่มีความเข้มข้นของแคลเซียมและแมกนีเซียมไอออนที่ละลายอยู่ในปริมาณสูง
แม้ว่าแร่ธาตุที่ทำให้เกิดความกระด้างเหล่านี้จะไม่เป็นอันตรายต่อสุขภาพของมนุษย์ แต่ก็สามารถก่อให้เกิดปัญหาต่างๆ มากมายทั้งในบ้านเรือนและอุตสาหกรรม ในบทความนี้เราจะสำรวจวิธีการวัด ทำความเข้าใจผลกระทบ และพิจารณาวิธีแก้ปัญหาที่ดีที่สุดในการจัดการหรือขจัดความกระด้างอย่างมีประสิทธิภาพ
น้ำกระด้าง (Hard Water) คืออะไร
น้ำกระด้างคือน้ำที่มีปริมาณแคลเซียม (Ca²⁺) และแมกนีเซียมไอออน (Mg²⁺) สูง โดยปกติแร่ธาตุเหล่านี้จะละลายในน้ำเมื่อไหลผ่านหิน เช่น หินปูน ชอล์ก หรือยิปซัม
ความกระด้างสามารถแบ่งได้เป็นสองประเภทหลัก:
- ความกระด้างชั่วคราว: เกิดจากแคลเซียมและแมกนีเซียมไบคาร์บอเนต; ขจัดออกได้โดยการต้ม
- ความกระด้างถาวร: เกิดจากแคลเซียมและแมกนีเซียมซัลเฟตหรือคลอไรด์; ไม่สามารถขจัดออกได้โดยการต้ม
ความกระด้างรวมโดยทั่วไปจะแสดงเป็นมิลลิกรัมต่อลิตร (มก./ล.) หรือส่วนในล้านส่วน (ppm) ของแคลเซียมคาร์บอเนต (CaCO₃) เทียบเท่า

ความกระด้างของน้ำคืออะไร
ความกระด้างของน้ำคือการวัดความเข้มข้นของไอออนบวกหลายค่าในน้ำ โดยเฉพาะอย่างยิ่งไอออนของแคลเซียมและแมกนีเซียม ไอออนเหล่านี้ละลายตามธรรมชาติจากหินและแร่ธาตุ เช่น หินปูน ชอล์ก และยิปซัม ขณะที่น้ำไหลผ่าน
หน่วยวัดน้ำกระด้างแสดงเป็น:
- มิลลิกรัมต่อลิตร (มก./ล.) ในรูปของแคลเซียมคาร์บอเนต (CaCO₃)
- ส่วนในล้านส่วน (ppm) (1 ppm = 1 มก./ล.)
- ระดับความกระด้าง (°dH หรือ °fH) ในบางพื้นที่

วิธีการวัดความกระด้างของน้ำ
มีหลายวิธีในการวัดความกระด้างของน้ำ ตั้งแต่การทดสอบภาคสนามอย่างรวดเร็วไปจนถึงการวิเคราะห์ในห้องปฏิบัติการที่แม่นยำ ลองมาสำรวจแต่ละวิธีกัน
1. การทดสอบสบู่ (วิธีง่ายๆ ในครัวเรือน)
การทดสอบสบู่เป็นวิธีแบบดั้งเดิมและง่ายในการประมาณค่าความกระด้างของน้ำ เป็นการประเมินเชิงคุณภาพ ไม่ใช่เชิงปริมาณ แต่ให้ภาพรวมคร่าวๆ
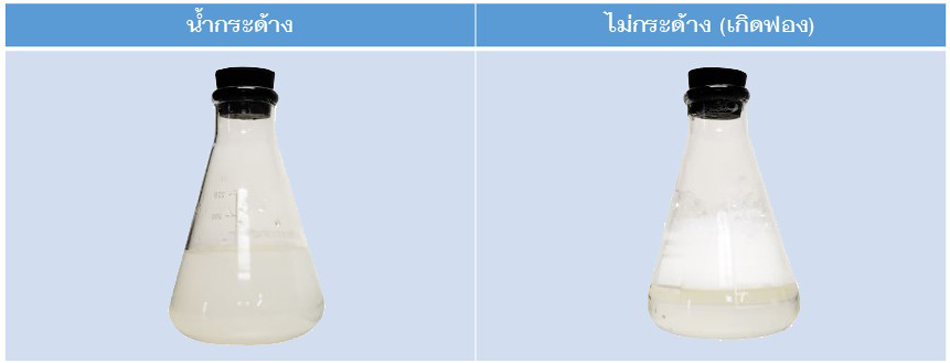
หลักการ: น้ำกระด้างไม่สามารถเกิดฟองได้ง่ายจากสบู่ เนื่องจากสบู่แคลเซียมหรือแมกนีเซียมที่ไม่ละลายน้ำ
ขั้นตอน:
- เติมน้ำตัวอย่างลงในขวดใสประมาณ 100 มิลลิลิตร
- เติมสบู่เหลวบริสุทธิ์ (ไม่ใช่ผงซักฟอก) สักสองสามหยด
- เขย่าขวดแรงๆ สักครู่
สังเกตผลลัพธ์:
- ฟองมากก่อตัวง่าย → น้ำอ่อน
- ฟองน้อยหรือไม่มีฟองและคราบ → น้ำกระด้าง
ข้อจำกัด:
- ไม่แม่นยำสำหรับการวิเคราะห์เชิงปริมาณ
- ไม่สามารถแยกความแตกต่างระหว่างความกระด้างชั่วคราวและถาวรได้
- ถึงกระนั้น ก็ยังเป็นวิธีการตรวจสอบเบื้องต้นที่มีประโยชน์สำหรับครัวเรือน
2.แถบทดสอบความกระด้างของน้ำ
วิธีที่ง่ายและประหยัดที่สุดสำหรับผู้ใช้ตามบ้าน ที่ไม่ต้องการผลออกมาเป็นตัวเลข และไม่ต้องการความแม่นยำ เป็นเพียงการตรวจประเมินในเบื้องต้น
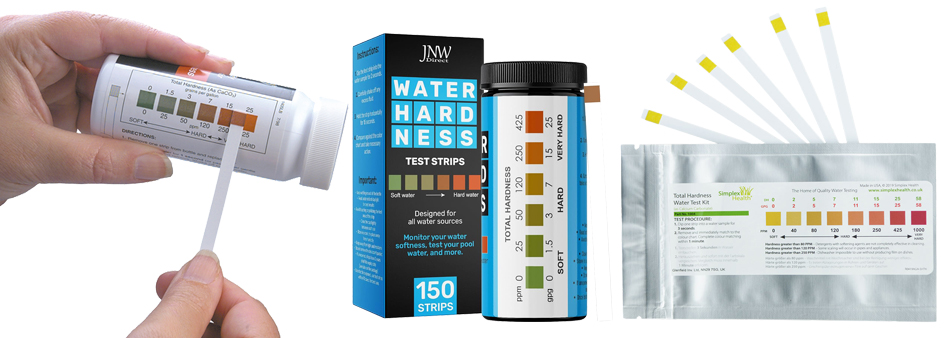
วิธีการทำงาน:
- ซื้อชุดทดสอบความกระด้างของน้ำ (หาซื้อได้ทางออนไลน์หรือที่ร้านฮาร์ดแวร์)
- จุ่มแถบทดสอบลงในแก้วน้ำประปาสักครู่
- นำแถบทดสอบออกและรอให้สีเปลี่ยน (ปกติ 10-30 วินาที)
- เปรียบเทียบสีกับตารางที่ให้มาในชุดทดสอบ
- แต่ละสีจะสัมพันธ์กับระดับความกระด้างของน้ำ (เช่น อ่อน ปานกลาง แข็ง)
ข้อดี: รวดเร็ว ราคาถูก และใช้งานง่าย
ข้อจำกัด: เป็นเพียงค่าประมาณเท่านั้น ไม่เหมาะสำหรับความแม่นยำในห้องปฏิบัติการ
3. วิธีการไทเทรต EDTA (วิธีมาตรฐานห้องปฏิบัติการ)
วิธีนี้เป็นวิธีที่แม่นยำและใช้กันอย่างแพร่หลายที่สุดในการหาค่าความกระด้างของน้ำทั้งหมดในห้องปฏิบัติการ

หลักการ:
EDTA (เอทิลีนไดอะมีนเตตราอะซิติกแอซิด) เป็นสารเชิงซ้อนที่ทำปฏิกิริยากับไอออนของแคลเซียมและแมกนีเซียมเพื่อสร้างสารเชิงซ้อนที่เสถียรและไม่มีสี จุดสิ้นสุดของการไทเทรตจะแสดงโดยการเปลี่ยนสีโดยใช้ตัวบ่งชี้
3.เครื่องวัดโดยใช้เครื่องวัด TDS (Total Dissolved Solids)
เครื่องวัดความกระด้างแบบอิเล็กทรอนิกส์ หรือ TDS (Total Dissolved Solids) จะให้ค่าการอ่านค่าแร่ธาตุแบบดิจิทัล

ขั้นตอน:
- เปิดเครื่องวัดและจุ่มหัววัดลงในแก้วน้ำ
- รอสักครู่เพื่อให้หน้าจอคงที่
- บันทึกค่าที่อ่านได้ (เป็น ppm หรือ mg/L)
การตีความ:
- แม้ว่า TDS จะรวมค่าของแข็งที่ละลายน้ำได้ทั้งหมด (ไม่ใช่แค่แร่ธาตุที่ทำให้เกิดความกระด้าง) แต่ค่า TDS ที่สูงมักจะบ่งชี้ว่าน้ำกระด้าง
ข้อดี: รวดเร็ว นำกลับมาใช้ใหม่ได้ แม่นยำสำหรับการวิเคราะห์ทั่วไป
ข้อจำกัด: ไม่สามารถแยกแคลเซียม/แมกนีเซียมได้โดยเฉพาะ
วิธีแก้ปัญหาน้ำกระด้าง
เมื่อทราบระดับความกระด้างแล้ว ก็สามารถใช้วิธีบำบัดได้หลายวิธี ขึ้นอยู่กับว่าความกระด้างนั้นเป็นแบบชั่วคราวหรือถาวร
1. การต้ม (สำหรับความกระด้างชั่วคราว)
การต้มจะขจัดความกระด้างชั่วคราวโดยการตกตะกอนของแคลเซียมและแมกนีเซียมคาร์บอเนต
ตัวอย่างปฏิกิริยา:
Ca(HCO3)2→CaCO3↓+H2O+CO2↑
อย่างไรก็ตาม การต้มไม่สามารถขจัดความกระด้างถาวรที่เกิดจากซัลเฟตและคลอไรด์ได้











